薬事関係法規の重要性
製薬業界で様々なポジションを経験した経験から、最も重要な教科はなにか解説します。
薬事関係法規の重要性
薬剤師の卵である薬学生の皆様、日々勉強お疲れさまです。
薬学生は勉強すべきことが沢山ありすぎて大変ですよね。
意外と好きな教科は勉強が頑張れたりするのですが、薬事関係法規は退屈に思った方も多いのではないでしょうか。
とにかく条文というかルールについて覚えていくだけ…
薬機法をベースに、薬剤師法など周辺法規を学びますが、覚えるばかりで興味を持ちにくいことは自身の経験からも納得できます。
現場の実感が無いからこそ、法規に対してイメージしにくく詰め込みの印象が強くなってしまいます。
ですが、現場に出たからこそ薬事の理解が重要だと気がつくことができました。
薬に関わる仕事において、ほぼすべての業務に薬事関係法規に基づいた行動が求められるからです。。
薬学生のアドバンテージ
どの職種においても薬学生には最大のアドバンテージがあると思っています。
当たり前ですが、薬事関係法規をまともに勉強する学科は医療系学科覗いてほぼありません。
薬機法の知識について、他の学生たちは入社後に研修で身につけますが、薬学生にとっては当たり前の素質なのです。
人が能力をつけて成長するのに、1→10は努力が必要ですが簡単です。
最も大変なのは0→1を作ること。薬学生はすでに土台ができている状態なのです。
病院、薬局では周りも全員薬剤師のため、アドバンテージを感じませんが一般企業は異ります。
また、薬事関係法規の基礎がわかる人材は、単にルールを知っているだけでなく倫理観も備えている人材として優位なのです。
研究職
研究職は創薬段階の最上流の職種です。
シーズ化合物などの探索段階は基礎研究部分は、比較的薬機法に縛られない業務が多いです。
しかし、動物実験などの非臨床試験の段階からは、薬機法を意識する必要があります。
信頼性の基準
大事な研究結果が疑われたり、信用できないものでは困るため、結果の取り扱いには一つの基準があります。
薬機法施行規則第43項に規定される『信頼性の基準』がその基準です。
正確性:試験結果に基づき、正確に作成されていること
完全性、網羅性:有効性・安全性等を疑わせる結果が得られた場合でも、当該結果について検討、記載されていること。(思わしくない結果を隠蔽していないこと)
保存性:根拠資料が適切に保存されていること
科学者として当たり前ではあるのですが、STAP細胞の小◯方さんの事態が起きていることもまた事実なのです。
GLP(Good Laboratory Practice)省令
GLP省令とは「医薬品の安全性に関する非臨床試験の実施の基準に関する省令」です。
簡単に表現するなら、確かな結果を保証するための実験室の管理レベル基準と言えます。
ひとつ、想像してみましょう。
試験を行うとき、その結果思わしくなかった場合は、操作の不備や機器の整備不良など”イレギュラー”を考えますよね。”試験環境”を整えることが、良い結果を得るのに必要なことだと考えることができます。
すると逆説的ですが、例えば手技や機器の不具合が懸念される点が1個でもあると、仮に好ましい結果が出たとしても、本当に真実かどうか疑わしくなってしまうのではないでしょうか。
GLP省令とは、信頼性の基準を満たすデータを取得するために、
・適切な手技レベルの担当者や試験施設や機器が揃っている
・組織体制や職員レベル、実験手順が明確
これらの管理基準や考え方をまとめたものです。
このような点が十分に反映されている施設での結果ならはじめて、確からしい結果だと保証されます。
従事する人材は、研究分野は多岐にわたるため、それぞれエキスパート人材が集うことになります。
したがっては薬学生が特別アドバンテージがあるわけではありません。
しかし研究とはいえ、創薬というフロー上のうえでは法律を意識する必要があるため、素養がある薬剤師には多くの活躍のチャンスがあるべきと思っています。
開発職
ひとくちに開発職といっても、化合物を医薬品として開発する行為に関わる全ての人が開発職といえます。
多岐に渡りますが、ここでは主に臨床試験に関する業務を行います。
GCP(Good Clinical Practice)省令
GCP省令とは「医薬品の臨床試験の実施の基準に関する省令」です。
GLP省令と似ていて、一言で言うなら臨床試験実施の際にが守るべき基準です。
世界中で医薬品開発の国際的なルールとなっているものを厚生労働省がまとめています。
GCP省令とは、治験に関する実施基準について書かれた省令で、実施そのもののルール、得られた結果の報告義務、IRB(治験審査委員会)やSMO(治験施設支援機関)の役割などが規定されています。
GCP省令に違反した場合は、データが信頼性の基準を満たしていないことになるだけでなく、治験の中止や新薬販売の中止などの措置がくだることもあります。
開発職に従事する薬剤師は全体に比してはそれほど多くありません。
データ処理や申請用資料をまとめる作業、医療従事者との調整では医療知識や倫理観が不可欠です。その素養を持つ薬剤師にはうってつけの職種と言えます。
薬事職
薬事職が役割が幅広く、会社毎の区分けもバラバラな状態です。
私なりに大きく3つに分類します。
・開発薬事:承認申請までの事務的な薬事業務
・薬制薬事:承認取得後の管理事務系な薬事業務
・CMC薬事:製造や分析に関わる実務系を薬事業務
と分類します。(会社毎に用語と職域がクロス、オーバラップしていることもあります)
開発薬事
新薬のための情報を集約して申請資料としてまとめあげ行政に提出します。途中、行政からの質問など窓口にもなる職種です。
申請資料は様式が決まっているので、フォーマットに当てはめるように資料をまとめていきます。
様々な資料を扱うため、医薬品開発の全容を理解している必要があり、多少の経験が必要です。
しかし悲観することなかれ、薬剤師であればその素養は十分あるように思います。
薬事関係法規や医薬品開発に関する知識も少なからず有しているからです。
申請資料には多少の”お作法的”な記載が必要です。レギュラトリーサイエンスという万人が共通理解できる科学的記載に則する部分がありますが、慣れればそれほど大変な作業ではありません。
開発薬事領域は様々な分野との調整が必要です。
資料の種類によって自分が要求することを伝えるためには、それぞれに理解が深いことを要求されます。薬剤師が開発薬事を担う意義があると言えます。
薬制薬事
薬制薬事は実際に医薬品として承認を受けたものを管理する薬事職と言えます。
承認を受けた医薬品は、メーカーが責任を持って製造販売していきます。
高い品質のものを恒常的に製造する義務が発生します。
医薬品が市販されると、治験段階とは比にならない規模の患者が使用することとなり、治験段階では表面化しなかった微細な副作用の発生に備える必要があります。
また市販後の本当に薬として効果があって有効なものなのかどうか、臨床試験を実施して再評価することも大事な作業です。
医薬品を流通させる面で、メーカーは品質にも責任を負います。
医薬品メーカーは製造販売業という薬機法上の許可が必要であり、運営には製造三役という薬機法上の役職人員を配置する必要があります。
GPSP(Good Post-marketing Study Practice)
GPSPとは「医薬品の製造販売後の調査及び試験の実施の基準」です。
市販後の使用規模に比べると、治験対象の人数はとても少ないといえます。
医薬品承認後は使用規模が拡大するため、治験段階には表面化しなかった副作用が発生する可能性があります。
また現場ニーズに実態に合わせた試験評価とすることで、医薬品の新たな価値、真の価値やポテンシャルを評価することが可能です。
医薬品開発段階では治験と呼びますが、承認後の医薬品を使用するため市販後臨床試験と呼ばれます。GPSPの目的はGVPに部分があり、内容としてはGCPに近い実施基準となっています。
製造三役
・総括製造販売責任者(総責):品責、安責をリードし全体品質を管理、判断する責任者
・品質保証責任者(品責):製造品質に関する管理の責任者
・安全管理責任者(安責):副作用、安全性情報収集に関する責任者
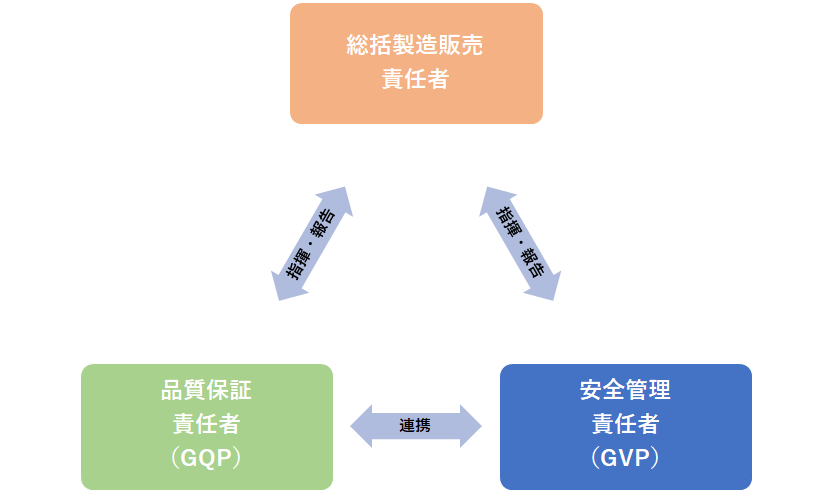
総括製造販売責任者
副作用情報の管理を担う安責と、製品品質を担う品責の意見を聞きながら品質担保をリードする役割です。
ここで特に、総責を務める要件が薬剤師であることに注目しなければなりません。
製造上の品質や、使用成績である副作用情報を加味しながら医薬品の品質の判断することは、多角的素地のある薬剤師にしかできない業務と言えます。
薬剤師以外は担えない領域として、最もアドバンテージが発揮できる職種であるにも関わらず、人材が大変不足しています。その理由は大きく2つあると考えます。
1つは製薬業界において当ポジションの重要性認識が高まらないからです。
研究・開発という大きな直接的利益を担う部門に比べ、安定供給、品質保証は直接的利益を期待する部門ではありせん。
そのため、企業という営利団体が注力すべき部門として軽視されがちであることが今なお課題となっています。
もう1つは、薬学教育において医薬費製造に関する薬剤師の活躍について、重きをおいていないからです。
薬学教育において優先されることは臨床現場で活躍する薬剤師の育成です。
医薬品供給という義務においては、製薬メーカーの品質保証部門は重大な役割であるはずが、医薬品製造に関するリスクマネジメントと合わせて、ポジションの重要性について、あまり多くの時間を割かれていないのが現状です。
品質保証責任者 GQP(Good Quality Practice)
品質保証責任者はGQPに則り、医薬品製造の品質管理を担っています。
GQP省令とは「医薬品、医薬部外品、化粧品及び医療機器の品質管理の基準に関する省令」であり、製造販売品質の保証基準のことを指します。
科学的根拠に基づいた品質管理が求めらます。
安全管理責任者 GVP(Good Vigilance Practice)
安全管理責任者はGVPに則り、販売後の副作用調査を継続しなければなりません。
GVP省令とは「医薬品製造販売後安全管理の基準に関する省令」であり、企業が整備すべき副作用調査体制に関する基準となっています。
品責、安責はいずれ総責を担う人材でもあるため、薬剤師が務めていることが喜ばしいといえます。
CMC薬事(Chemistry, Manufacturing and Control)
CMC薬事とは、医薬品製造、分析に関わる実務管理を担う薬事職となります。
医薬品製造において、製品自体の特性や評価方法を決める必要があります。
具体的には原薬・製剤の化学的特性、製剤開発、製造方法の検討、品質規格の設定、分析法開発などです。
なぜ、そんなことをするのか…
検証された方法通りに作った製品を、検討された方法分析することで一定の品質が保たれていることが保証されます。
医薬品の安定供給においては、継続的に製造され、品質が保たれていることを継続的に担保する必要あるからです。
例えば途中、材料が廃番となり別のメーカー品に切り替えが必要になったとき、その変更が全体品質に影響が無いことを検証しなければなりません。
無事に問題ないことが検証された後、製造販売承認書の変更作業などが発生します。
このような変更作業に対応するのがCMC薬事職と言えます。(※実務作業と事務作業の境界など会社によって様々な場合があります)
CMC薬事においては、医薬品の化合物としての科学的評価が求められます。
ものづくり上の物理的観点、化学品混合における科学的見解の素地など、やはり多角的視点の要求される職種と言えます。
多角的素地こと薬剤師の最大の強みであるため、活躍のチャンスが大いにある職種と言えます。
多くの場合、向上で製造実務経験を積んだ後にCMC薬事職へステップアップする傾向が多いのが特徴です。しかし素地のある薬剤師であるならば、何年もの現場鍛錬は必要無いように思います。
製造部門職
製造部門は医薬品製造工場で医薬品の製造を担います。
製造方法の検討から、スケールアップ検討、承認申請に向けた試験法作成など、開発に関わる部門もありますが、多くの場合は承認された品目の製造であり、製造部門が最も対応すべき重要な薬事関係法規といえばGMPです。
GMP(Good Manufacturing Practice)
GMPとは「医薬品の製造及び品質管理に関する基準」です。
製造業者に求められる適正な製造規範のことを指しています。
品質管理として、原材料の入荷から、製造、包装、保管や出荷、場合によって回収処理までに係る業務を規定するものとなっています。
製造管理者という責任者を配置することが規定され、医薬品製造管理者は薬剤師でなければなりません。
製造販売業の三役体制のように、製造所においても製造管理者を長として、製造部門と品質部門を統括します。
製造部門が適切な手順で製造した実績を示し、品質部門はその製品の分析結果から品質に問題が無いことを検証します。
具体的業務は標準作業手順書(SOP)として標準化され、実際の製造指図から、工場管理や品質管理の基準書などが設定され、高い管理レベルで医薬品製造が実施されることを担保する為の基準となっています。
品質と一口に行っても具体的なものづくりの作業手順から、衛生管理思想まで、多様な視点からの品質担保が求められます。
科学者としての素養から、実際に人が服用する倫理観を含めた大局的視野が求められる部分もあり、薬剤師の素養が生きる職種であると言えます。
MR(Medical Representative):医薬情報担当者
医薬情報担当者は医療従事者に新薬の説明や情報提供をして、臨床使用機会を創出してきます。
営業職と言えますが、売買に関する交渉はせず、使用拡大を担う情報提供を主な業務としています。
もう1つ大きな役割は、医療現場に情報提供と同時に、使用成績として副作用が発生した場合は、その情報を収集する役割を担っています。
まとめ
創薬に関わる様々な職種がありますが、それぞれが薬事関係法規をベースの業務が求められます。
一言で薬事関係法規といってもそれぞれが対応すべき法規が異なり、職種を超えたキャリアアップも難易度が上がります。
しかし、何度も記載するように薬剤師には多角的素地があり、領域を超えたキャリアアップにも可能性や期待も大きいものであるはずです。
薬剤師のキャリアは千差万別です。
しかもキャリアチェンジを可能とする下地があり、その鍵となるのが薬事関係法規です。
しかし残念ながら、多くの場合薬剤師側にも自覚がありません。キャリアや就職に悩んだとき、前向きな自信をもたせてくれるのが薬事関係法規であり、最も重要な科目である理由です。




